アイトラッキング、脳波(EEG)、筋電図(EMG)、表情分析、皮膚電気反応(GSR)といった最新の診断ツールが、いかにして医療診断のあり方を変革しつつあるかをご紹介します。本ブログでは、これらの技術が神経疾患や精神疾患の微細なバイオマーカーをどのように解明し、より迅速で、より利用しやすく、データに基づいたアプローチを通じて、早期発見と臨床判断の向上を実現しているかを探ります。
Table of Contents
診断こそが医療の始まりである。迅速かつ容易に正確な診断を下すことは、言うまでもなく医学の中心的な目標である。なぜなら、それによって患者には適切な治療をできるだけ早く受けられるという利益がもたらされ、診断を行う医師にとっても時間を節約できるため、より多くの患者を診ることができるようになるからである。
医療診断もまた多額の費用がかかるものであり、医療費全体の約10%が診断に充てられており、この割合は今後数年間でさらに増加していく見込みです。信頼性の高い医療検査の利便性、利用しやすさ、そして手頃な価格を実現する方法を模索することは、明らかに追求すべき価値ある目標です。
診断の向上にはいくつかのアプローチがあるが、この分野における変化の主な原動力の一つは技術である。HarezlakとKasprowskiが最近の論文で述べているように、「医療処置や治療の成果と質は、技術の発展と密接に結びついている」[1]。多くの分野と同様、技術ができることが増えれば増えるほど、私たちにもできることが広がるのである。
技術の進歩により、機器の設計や仕様だけでなく、その内部に組み込まれたソフトウェアも進化を遂げています。これにより、新たな技術革新が診断業務の負担軽減に寄与する絶好の機会が生まれました。まだ多くの研究が必要ではありますが、アイトラッカー、脳波(EEG)、筋電図(EMG)、心電図(ECG)といった機器が、疾患や障害の早期発見にどのように貢献できるかについて、その兆しが見え始めています。
以下では、これらの技術を応用して診断の精度と利用可能性の両方を向上させる方法についていくつか解説します。ここでは主に、原因が直接特定されている他の疾患に比べ、神経疾患や精神疾患の診断は曖昧になりがちなため、今後の研究において、こうした疾患のバイオマーカーをいかに確実に特定できるかに焦点を当てます。
アイトラッキング
医学的診断の文脈でアイトラッカーを用いた最初の研究の一つは、100年以上前の1908年に実施された[2]。「ドッジ・フォトクロノグラフ」――角膜の反射を撮影する手法――を用いて、数字を視認した際の眼球運動が記録された。その結果、一貫性には欠けるものの、統合失調症患者の眼球速度は、統合失調症ではない対照群とは異なっていることが判明した。

ディーフェンドルフとドッジ、1908年。
それ以来、アイトラッカーの使いやすさ、精度、そして手頃な価格は、劇的に向上しました。
アイトラッキングの研究により、健常者と、統合失調症[3]、双極性障害[4]、軽度認知障害(MCI)[5]、アルツハイマー病[6]、多発性硬化症[7]、自閉症[8, 9]、パーキンソン病[10]、およびADHD[10, 11]の患者との間に、顕著な違いが明らかになった。
アイトラッカーを用いて視覚行動を測定するために、一般的に用いられる実験的パラダイムはいくつかある。最も一般的なアプローチの一つが、プロサッカード課題とアンチサッカード課題である。
サッカード前課題は比較的単純で、通常、被験者が画面上の中央の固定点を注視し、刺激が現れたら視覚的にそれに注意を向けるというものです。パーキンソン病の診断を受けていない人々と比較して、パーキンソン病患者では反応時間の遅延(反応時間の延長)が認められています [10]。
サッカード抑制課題も同様の仕組みですが、被験者には刺激が現れた際に、その反対方向を見るよう指示されます。この手法を用いると、MCI(アルツハイマー病の前段階と考えられる状態[12])の患者において顕著な差異が認められます。彼らは指示された方向を見る際の反応時間が長く、誤答する傾向が強いのです[13]。
アイトラッキング検査は、比較的低コストで、身体への負担が少なく、検査の準備も簡単であるため、視覚行動に影響を及ぼすさまざまな疾患を迅速に検査するために、容易に導入できると想像に難くない。
脳波

脳波(EEG)の活動とてんかんとの関連性を示す研究は数多く存在する[14]、 アルツハイマー病[15]、自閉症[16]、ADHD[17]、統合失調症[18]、双極性障害[19]、強迫性障害[20]、さらにはクロイツフェルト・ヤコブ病[21]など[22]との関連性を示す研究は数多く存在する。
前述の通り、これらの疾患の多くは、アイトラッキングによる評価の結果、視覚行動に影響を及ぼすことが明らかになっています。今後の研究では、こうした関連性が示唆される知見をさらに掘り下げることで、新たな知見が得られる可能性があります。
脳波(EEG)は脳活動を直接測定する手法であるため、神経疾患や障害の調査に適したツールであることは、おそらく驚くべきことではない。しかし、関連する論文では、脳波による所見の一部について、その信頼性が疑問視されることもある。他の手法を併用することや、全般的なさらなる研究が進むことで、より明確な理解が得られる可能性があるようだ。
脳波検査(EEG)のセットアップには、電極の適切な位置の決定、ゲルの塗布、インピーダンスの確認など、ある程度の作業が必要ですが、こうしたシステムのセットアップの容易さは、ここ数年で向上しています。さらに、医療現場において脳波検査が現在広く普及していることから、必要に応じて診断の場面でこの技術をさらに活用するためのシステムやトレーニング体制は、すでに整っています。
筋電図
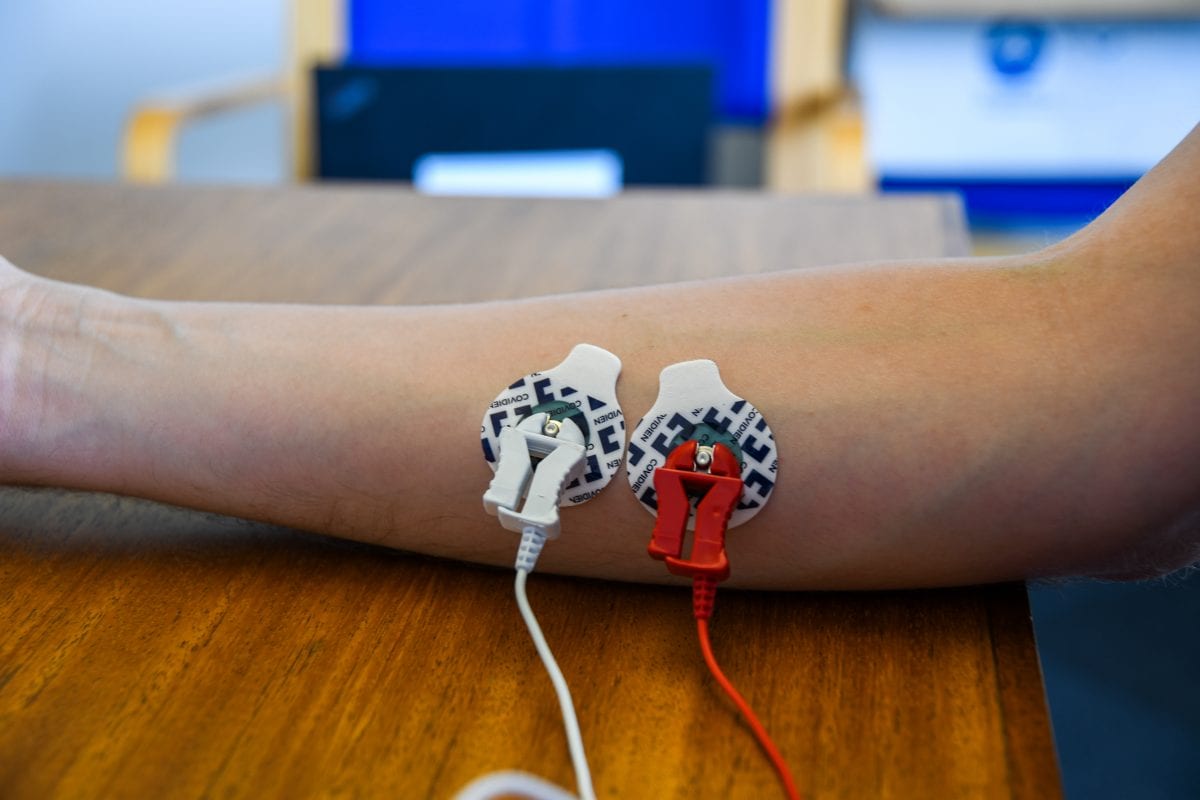
筋活動を測定する方法として、筋電図(EMG)を用いた研究により、筋肉の発達や機能に影響を及ぼすさまざまな疾患(例えばポンペ病[23])との関連性が明らかにされてきた。しかし、EMGが一部の神経疾患の指標としても活用できる可能性があるという兆候が見られている。
研究によると、パーキンソン病[24]とハンチントン病[25]の患者の間で、筋電図(EMG)記録に有意な違いが認められている。これらはいずれも、主に脳に影響を及ぼす進行性の変性疾患である(ただし、脳に限られるわけではなく、両疾患とも筋症状を伴う)。今後の研究により、異常な筋電図記録と疾患との関連性が明らかになり、診断への新たな手がかりとなる可能性がある。
EMG装置は、非侵襲的であり、多くの場合携帯可能ではあるものの、セットアップにはある程度の手間(皮膚の準備や筋活動のベースライン記録など)を要します。しかし、EEGと同様、これらの装置はすでに臨床現場で広く活用されています。
表情分析
表情の生成は、多くの場合、自動的で無意識のプロセスであるが、意識的に制御することも可能である。自閉症の人々においては、表情を作る能力に違いが見られることが分かっている[31]。
また、自閉症のある人の社会的スキルを向上させるための訓練の文脈においても、表情分析は広く議論されている[32]。自閉症の診断とは直接的な関連はないものの、こうしたシステムから得られる知見は、自閉症の発症メカニズムの理解を深める一助となり得る。
研究者らは、自動顔面表情解析を用いて統合失調症の特徴を特定する手法を提案している[33]。統合失調症は、感情表現の障害や感情の平板化と関連することが多く、その結果、患者の顔面表情は統合失調症でない対照群と比較して異なる可能性がある。研究者らは、このシステムが両群間に有意な違いを識別できることを確認しており、診断を支援するツールとしてさらに開発が進められる可能性がある。

自動化された表情分析は、全く目立たないため、患者に不快感を与えることなく実施することができます。自閉症や精神疾患との関連性を明確に解明するにはさらなる研究が必要ですが、その使いやすさから、この手法は臨床現場ですぐに活用できる可能性があります。
同様に、人間の声もまた、神経疾患や精神疾患を理解するための、目立たずかつ貴重なデータ源となります。医療診断の新たな分野としての**音声分析**の可能性について、詳しくご覧ください。
皮膚電気反応
GSR(皮膚電気反応)は、EDA(皮膚電気活動)とも呼ばれ、汗腺の活動を測定する指標であり、多くの場合(ただし、必ずしもそうとは限らないが)、指から測定される。この方法は実施が容易であり、測定機器は携帯可能なため、自然な状態でデータを収集することができる。
(表情分析と同様に)統合失調症との関連も指摘されているが、診断分類の違いに起因する可能性のある不一致も見られる [27, 28]。今後の研究により、GSR/EDAが統合失調症の診断において有用な情報を提供できるかどうか、またその仕組みが明らかになるかもしれない。
個人が経験しているストレスのレベル(心電図(ECG)で測定された心拍数と併せて)との間に、有意な関連性が認められている[26]。これは精神疾患ではないものの、臨床の現場において収集すべき有益な情報である可能性がある。

同様に、自閉症の指標としてのGSR/EDAについても一貫性のない結果が報告されている[29]が、信頼性が高く実用可能なバイオマーカーを特定するため、大規模な研究プロジェクトが現在も進められている[30]。以前にも触れたJAKE研究プロジェクトは、EEG、表情分析、GSR、アイトラッキングデータから得られた知見や、それらが自閉症とどのように関連しているかについて、さらなる洞察をもたらす一助となる可能性がある。
GSR/EDAデバイスは装着が容易で、比較的安価であり、日常の動作にほとんど支障をきたすことなく携帯型デバイスとして着用できます。これにより、精神疾患との関連性をさらに調査するための、移動中の自然な状態でのデータ収集が可能となるでしょう。
結論
こうしたデバイスの大きな利点は、各デバイスからのデータを同時に収集できる点にある。複雑なデータセットに対する機械学習手法の普及に伴い、こうした分析が、さまざまな潜在的な疾患や障害のより自動化された評価への道を開くことになるだろうことは容易に想像できる。
これらの手法を組み合わせることで、個々の結果の信頼性をさらに高めることができる(例えば、EEGとアイトラッキングデータの分析により自閉症児の早期診断を行うこと。予備的な結果によれば、このアプローチには価値があることが示唆されている[34])。
上記の研究は、これらのデバイスから収集されたデータと神経疾患や障害との間に潜在的な関連性が認められた事例のほんの一部に過ぎません。多くの場合、決定的なバイオマーカーを特定するにはさらなる研究が必要ですが、現在の研究の進展は、これが我々が向かっている方向であることをはっきりと示しています。
さまざまなセンサーが、神経疾患や精神疾患の解明にどのように役立つかについて、お読みいただきありがとうございました。iMotionsが医療・ヘルスケア研究における課題の理解を深めるためにどのように貢献できるか、詳しくはこちらをご覧ください。
参考文献
[1] Harezlak, K., Kasprowski, P. (2018). 医学におけるアイトラッキングの応用:調査、研究課題および課題. Computerized Medical Imaging and Graphics. 4月; 65:176-190.
[2] Diefendorf, A. R., Dodge, R. (1908). 写真記録に基づく精神障害者の眼球反応に関する実験的研究. Brain, 第31巻第3号, 451–489頁, Https://Doi.Org/10.1093/Brain/31.3.451
[3] Arolt, V., Lencer, R., Nolte, A., Müller-Myhsok, B., Purmann, S., Schürmann M., et al. (1996). 視線追跡機能障害は統合失調症の推定される表現型感受性マーカーであり、同疾患の多発家系において6番染色体p腕上の遺伝子座にマッピングされる。Am. J. Med. Genet. 67:564–579.
[4] Garcıa-Blanco, A., Salmerón, L., Perea, M., Livianos, L. (2014). 双極性障害の各エピソードにおける感情的な画像に対する注意の偏り:アイトラッキング研究. Psychiatry Res. 215 (3), 628–633.
[5] Yang, Q., Wang, T., Su, N., Xiao, S., Kapoula, Z. (2013). 軽度から中等度のアルツハイマー病患者および記憶障害型軽度認知障害患者における特定のサッカード障害. Age. 35 (4), 1287–1298.
[6] Crutcher, M. D., Calhoun-Haney, R., Manzanares, C. M., Lah, J. J., Levey, A. I., Zola, S. M. (2009). 視覚的ペア比較課題中の視線追跡が早期認知症の予測因子としての役割。Am. J. Alzheimer’s Dis. Other Dementias.
[7] Derwenskus, J., Rucker, J.C., Serra, A., Stahl, J. S., Downey, D. L., Adams, N. L., Leigh, R. (2005). 「異常な眼球運動は多発性硬化症における障害を予測する:2年間の追跡調査」『Ann. N. Y. Acad. Sci.』1039 (1), 521–523.
[8] Wang, S., Jiang, M., Duchesne, X.M., Laugeson, E.A., Kennedy, D.P., Adolphs, R., Zhao, Q. (2015). モデルベースのアイトラッキングによる自閉症スペクトラム障害における非定型的な視覚的顕著性の定量化. Neuron. 88 (3), 604–616.
[9] Jones, W., Carr, K., Klin, A. (2008). 接近してくる大人の目への優先的な視線向きの欠如は、自閉症スペクトラム障害を持つ2歳児の社会的障害の程度を予測する。Arch. Gen. Psychiatry. 65 946–954. 10.1001/archpsyc.65.8.946
[10] Tseng, P.-H., Cameron, I. G., Pari, G., Reynolds, J. N., Munoz, D. P., Itti, L. (2013). 自然な視線運動に基づく臨床集団の高スループット分類. J. Neurol. 260 (1), 275–284.
[11] Dankner, Y., Shalev, L., Carrasco, M., Yuval-Greenberg, S. (2017). 注意欠陥・多動性障害(ADHD)を有する成人とそうでない成人におけるサッカードの前刺激抑制:時間的予測の指標として. Psychological Science. 28(7), 835–850.
[12] Petersen, R. (2009). アルツハイマー病の早期診断:軽度認知障害(MCI)の段階ではすでに手遅れなのか? Current Alzheimer Research. 6(4):324–330. doi: 10.2174/156720509788929237.
[13] Pereira, M. L., Camargo, M., Aprahamian, I., Forlenza, O. V. (2014). 眼球運動解析と認知処理:アルツハイマー病への移行を示す指標の検出. Neuropsychiatr Dis Treat. 10:1273–1285. doi: 10.2147/NDT.S55371.
[14] Mormann, F., Kreuz, T. H., Rieke, C. H., Andrzejak, R. G., Kraskov, A., David, P., Elger, C. E., Lehnertz, K. (2005). てんかん発作の予測可能性について. Clin Neurophysiol. 116:569–97.
[15] Kowalski, J. W., Gawel, M., Pfeffer, A., Barcikowska, M. (2001). アルツハイマー病における脳波検査の診断的価値:精神機能障害の重症度との相関. Journal of Clinical Neurophysiology. 18(6): 570–575.
[16] Cociu, B. A., Das, S., Billeci, L., Jamal, W., Maharatna, K., Calderoni, S., Narzisi, A., Muratori, F. (2017). 自閉症における多模態機能的および構造的脳接続性の解析:EEG、fMRI、およびDTIを用いた予備的な統合的アプローチ. IEEE Trans. Cogn. Develop. Syst. 10, 2, 213-226. DOI: 10.1109/TCDS.2017.2680408.
[17] Arns, M., Conners, C. K., Kraemer, H. C. (2013). ADHDにおけるEEGのシータ波/ベータ波比に関する10年間の研究:メタ分析. J. Atten. Disord. 17, 374–383. 10.1177/1087054712460087.
[18] Boutros, N. N., Arfken, C., Galderisi, S., Warrick, J., Pratt, G., Iacono, W. (2008). 統合失調症の診断検査としてのスペクトル脳波異常の現状. Schizophr. Res. 99, 225–237.
[19] Kam, J. W., Bolbecker, A. R., O’Donnell, B. F., Hetrick, W. P., Brenner, C. A. (2013). 双極性障害および統合失調症における安静時脳波(EEG)のパワーおよびコヒーレンスの異常. J Psychiatr Res. 47:1893–901. doi: 10.1016/j.jpsychires.2013.09.009.
[20] Velikova, S., Locatelli, M., Insacco, C., Smeraldi, E., Comi, G., Leocani, L. (2010). 強迫性障害における脳回路の機能障害:EEGリズムのソース解析およびコヒーレンス解析. Neuroimage. 49(1):977–983.
[21] Zerr, I., Pocchiari, M., Collins, S., Brandel, J. P., de Pedro, C. J., Knight, R. S., et al. (2000). クロイツフェルト・ヤコブ病の診断補助としての脳波および脳脊髄液中の14-3-3タンパク質の解析. Neurology. 55:811–815. doi: 10.1212/WNL.55.6.811.
[22] Herrmann, C., Demiralp, T. (2005). 神経精神疾患におけるヒトのEEGガンマ波動. Clin. Neurophysiol. 116, 2719–2733. doi: 10.1016/j.clinph.2005.07.007
[23] Kishnani, P. S., Steiner, R. D., Bali, D., Berger, K., Byrne, B. J., Case, L., Crowley, J. F., Downs, S., Howell, R. R., Kravitz, R. M., Mackey, J., Marsden, D., Martins, A. M., Millington, D. S., Nicolino, M., O’Grady, G., Patterson, M. C., Rapoport, D. M., Slonim, A., Spencer, C. T., Tifft, C. J., Watson, M. S. (2006). ポンペ病の診断および管理ガイドライン. Genet Med. 8:267–288. doi: 10.1097/01.gim.0000218152.87434.f3.
[24] Vitale, C., Marcelli, V., Furia, T., et al. (2011). 体幹の側方屈曲を示すパーキンソン病患者における前庭機能障害と適応性姿勢失調. Mov Disord. 26:1458-1463.
[25] Swerdlow, N. R., Paulsen, J., Braff, D. L., et al. (1995). ハンチントン病患者における聴覚および触覚性驚愕反応のプレパルス抑制障害. J. Neurol. Neurosurg. Psychiatry. 58, 192–200.
[26] Tulen, J. H. M., Moleman, P., Van Steenis, H. G., Boomsma, F. (1989). ストループ色語課題に対するストレス反応の特性化。Pharmacol. Biochem. Behav. 32 9–15. 10.1016/0091-3057(89)90204-9.
[27] Öhman, A. (1981). 皮膚電気活動と統合失調症の感受性:総説. Biol. Psychol. 12, 87–145. 10.1016/0301-0511(81)90008-9.
[28] Zahn, T. P., Frith, C. D., Steinhauer, S. R. (1991). 統合失調症における自律神経機能:皮膚電気活動、心拍数、瞳孔反応. S.R. Steinhauer, J. H. Gruzelier, & J. Zubin (編), 『統合失調症ハンドブック:第5巻 神経心理学、心理生理学、および情報処理』(pp. 185-224)所収。アムステルダム:エルゼビア。
[29] Hirstein, W., Iversen, P., Ramachandran, V. S. (2001). 自閉症児における人や物体に対する自律神経反応. Proc Biol Sci. 268(1479):1883–8.
[30] Ness, S. L., Manyakov, N. V., Bangerter, A., et al. (2017). JAKE(R) マルチモーダルデータ収集システム:自閉症スペクトラム障害に関する観察研究からの知見. Front Neurosci. 11:517.
[31] Manfredonia, J., Bangerter, A., Manyakov, N. V., Ness, S., Lewin, D., Skalkin, A., Boice, M., Goodwin, M. S., Dawson, G., Hendren, R., Leventhal, B., Shic, F., Pandina, G. (2018). 自閉症スペクトラム障害を有する個人における意図的な感情的表情の自動認識. J Autism Dev Disord. 10月8日. doi: 10.1007/s10803-018-3757-9.
[32] Liu, R., Salisbury, J. P., Vahabzadeh, A., Sahin, N. T. (2017). 自閉症に焦点を当てた拡張現実スマートグラスシステムによる社会的コミュニケーションおよび行動指導の実現可能性. Front. Pediatr. 5:145. doi: 10.3389/fped.2017.00145.
[33] Wang, P., Barrett, F., Martin, E., Miloncva, M., Gur, R. E., Gur, R. C., et al. (2008). 神経精神疾患の自動動画ベースの表情分析. Journal of Neuroscience Methods. 168: 224–238.
[34] Billeci, L., Narzisi, A., Tonacci, A., Sbriscia-Fioretti, B., Serasini, L., Fulceri, F., Apicella, F., Sicca, F., Calderoni, S., Muratori, F. (2017). 自閉症スペクトラム障害における共同注意の反応および開始の研究に向けた、脳波(EEG)とアイトラッキングの統合的アプローチ. Scientific Reports, 7(1):13560.



