Die Diagnose ist der Ausgangspunkt der Medizin. Eine schnelle und einfache Erstellung der richtigen Diagnose ist aus offensichtlichen Gründen ein zentrales Ziel der Medizin: Sie kommt dem Patienten zugute, indem sie sicherstellt, dass er so schnell wie möglich die richtige Behandlung erhält, und spart dem Diagnostiker Zeit, sodass er sich um mehr Patienten kümmern kann.
Auch die medizinische Diagnostik ist eine kostspielige Angelegenheit: Rund 10 % aller medizinischen Kosten entfallen auf die Diagnostik, und dieser Anteil wird in den kommenden Jahren weiter steigen. Es ist zweifellos ein lohnenswertes Ziel, Wege zu finden, um zuverlässige medizinische Tests einfacher, zugänglicher und erschwinglicher zu machen.
Es gibt verschiedene Ansätze zur Verbesserung der Diagnostik, doch einer der wichtigsten Triebkräfte für Veränderungen in diesem Bereich ist die Technologie. Wie Harezlak und Kasprowski in einem kürzlich erschienenen Artikel feststellen: „Die Leistungsfähigkeit und Qualität medizinischer Verfahren und Behandlungen sind untrennbar mit der technologischen Entwicklung verbunden“ [1]. Wie in vielen anderen Bereichen gilt auch hier: Je mehr die Technologie leisten kann, desto mehr können wir leisten.
Der technologische Fortschritt hat nicht nur zu Verbesserungen beim Design und bei den technischen Daten der Geräte geführt, sondern auch bei der darin enthaltenen Software. Dies bietet eine hervorragende Gelegenheit, durch neue technologische Errungenschaften die Belastung durch diagnostische Arbeiten zu verringern. Auch wenn noch viel Forschungsarbeit zu leisten ist, gibt es bereits Anzeichen dafür, wie Geräte wie Eye-Tracker, EEG, EMG und EKG zur Früherkennung von Krankheiten und Störungen beitragen können.
Im Folgenden werden einige Möglichkeiten aufgezeigt, wie diese Technologien eingesetzt werden können, um sowohl die diagnostische Genauigkeit als auch die Verfügbarkeit zu verbessern. Der Schwerpunkt liegt dabei vor allem darauf, wie zukünftige Forschungsarbeiten Biomarker für neurologische Erkrankungen oder psychiatrische Störungen zuverlässig identifizieren könnten, da die Diagnose in diesen Fällen oft weniger eindeutig ist als bei anderen Krankheiten, bei denen eine Ursache direkt identifiziert wurde.
Eye-Tracking
Eine der ersten Studien, bei der ein Eye-Tracker im Rahmen der medizinischen Diagnostik zum Einsatz kam, fand vor über hundert Jahren, im Jahr 1908, statt [2]. Mithilfe des „Dodge-Photochronographen“ – einer Methode zur fotografischen Erfassung der Reflexion der Hornhaut – wurden die Augenbewegungen beim Betrachten von Ziffern aufgezeichnet. Es zeigte sich, wenn auch nicht durchgängig, dass sich die Augenbewegungsgeschwindigkeit bei Schizophrenen von derjenigen der nicht-schizophrenen Kontrollgruppe unterschied.

Diefendorf und Dodge, 1908.
Die Benutzerfreundlichkeit, Genauigkeit und Erschwinglichkeit von Eye-Trackern hat sich seitdem erheblich verbessert.
Eye-Tracking-Untersuchungen haben erhebliche Unterschiede zwischen Kontrollgruppen und Menschen mit Schizophrenie [3], bipolarer Störung [4], leichter kognitiver Beeinträchtigung (MCI) [5], Alzheimer-Krankheit [6], Multipler Sklerose [7], Autismus [8, 9], Parkinson-Krankheit [10] und ADHS [10, 11] aufgezeigt.
Es gibt verschiedene experimentelle Paradigmen, die üblicherweise zur Untersuchung des Blickverhaltens mit Eye-Trackern eingesetzt werden. Zu den gängigsten Ansätzen zählen Pro- und Anti-Sakkaden-Aufgaben.
Pro-Sakkaden-Aufgaben sind relativ einfach – in der Regel müssen die Teilnehmer dabei auf einen zentralen Fixationspunkt auf einem Bildschirm starren und dann ihre Aufmerksamkeit auf einen Reiz richten, sobald dieser erscheint. Bei Menschen mit Parkinson-Krankheit wurden im Vergleich zu Menschen ohne Parkinson-Diagnose längere Reaktionszeiten festgestellt [10].
Anti-Sakkaden-Aufgaben sind ähnlich, allerdings wird der Teilnehmer angewiesen, in die entgegengesetzte Richtung zum Reiz zu blicken, wenn dieser erscheint. Dieser Ansatz hat signifikante Unterschiede bei Menschen mit MCI (einem wahrscheinlichen Vorläufer der Alzheimer-Krankheit [12]) aufgezeigt, die beim Blick in die geforderte Richtung längere Reaktionszeiten aufweisen und häufiger Fehler machen [13].
Angesichts der relativen Erschwinglichkeit, der Nicht-Invasivität und der einfachen Durchführung ist es leicht vorstellbar, dass Eye-Tracking-Tests problemlos eingesetzt werden könnten, um schnell eine Reihe von Erkrankungen zu untersuchen, die das Sehverhalten beeinflussen.
EEG

Es mangelt nicht an Studien, die einen Zusammenhang zwischen der EEG-Aktivität (Elektroenzephalografie) und Epilepsie [14], der Alzheimer-Krankheit [15], Autismus [16], ADHS [17], Schizophrenie [18], bipolaren Störungen [19], Zwangsstörungen [20] und sogar der Creutzfeldt-Jakob-Krankheit [21] sowie weiteren Erkrankungen [22].
Wie bereits erwähnt, hat sich gezeigt, dass viele dieser Erkrankungen Auswirkungen auf das Sehverhalten haben, wie durch Eye-Tracking-Untersuchungen festgestellt wurde. Weitere Forschungen könnten davon profitieren, diese potenziell damit zusammenhängenden Befunde zu untersuchen.
Es ist vielleicht keine Überraschung, dass das EEG als direkte Methode zur Messung der Gehirnaktivität ein geeignetes Instrument zur Untersuchung neurologischer Erkrankungen und Störungen ist. Allerdings wird die Aussagekraft einiger EEG-Befunde in den entsprechenden Artikeln mitunter in Frage gestellt. Es scheint, dass der kombinierte Einsatz anderer Methoden sowie weitere Forschung im Allgemeinen dazu beitragen könnten, mehr Klarheit zu schaffen.
Zwar erfordert die Einrichtung eines EEG-Systems einen gewissen Aufwand (Bestimmung der richtigen Position der Elektroden, Auftragen von Gel, Überprüfung der Impedanz usw.), doch hat sich die Handhabung solcher Systeme im Laufe der Jahre vereinfacht. Hinzu kommt, dass die derzeitige breite Anwendung des EEG im medizinischen Bereich bedeutet, dass die Systeme und die entsprechende Ausbildung bereits vorhanden sind, um diese Technologie bei Bedarf auch in diagnostischen Kontexten einzusetzen.
EMG
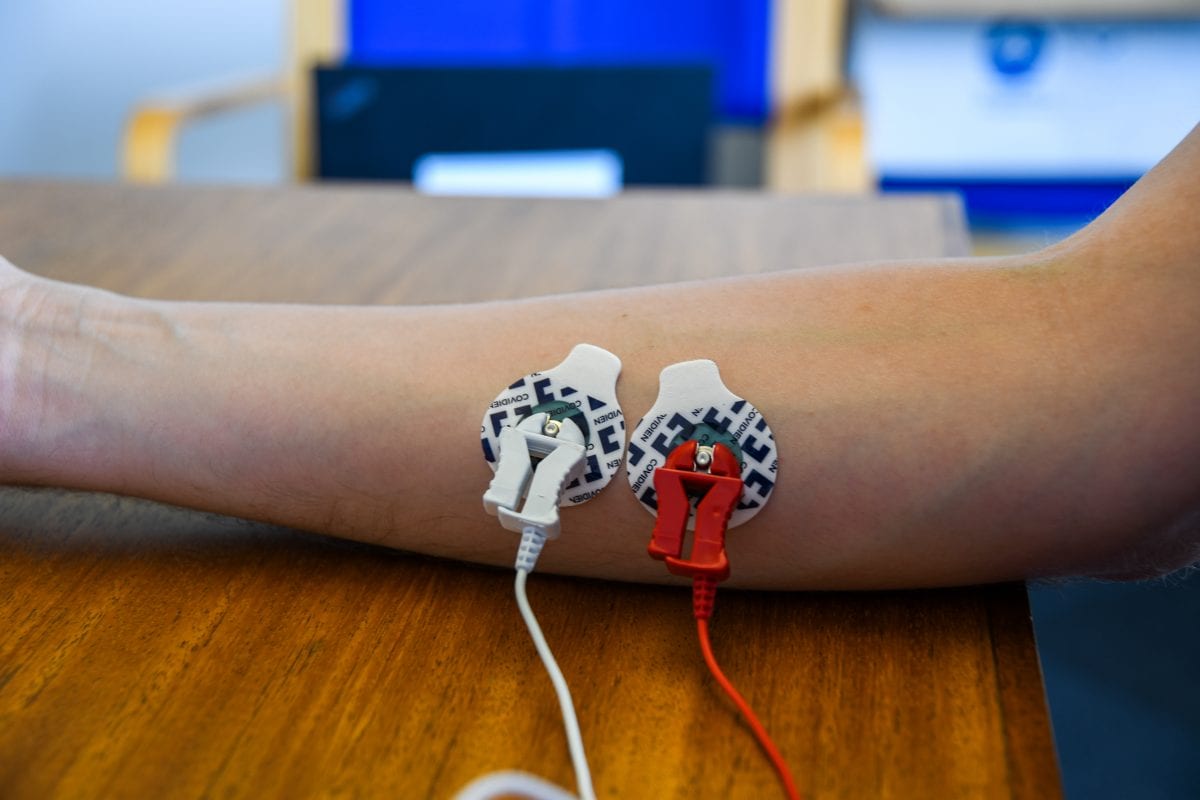
Als Methode zur Messung der Muskelaktivität hat die Forschung mittels EMG (Elektromyographie) natürlich Zusammenhänge zwischen einer Vielzahl von Erkrankungen aufgezeigt, die die Muskelentwicklung und -funktion beeinträchtigen (z. B. die Pompe-Krankheit [23]). Es gibt jedoch Anzeichen dafür, dass das EMG sogar als Indikator für bestimmte neurologische Erkrankungen dienen kann.
Untersuchungen haben signifikante Unterschiede bei den EMG-Aufzeichnungen zwischen Patienten mit Parkinson-Krankheit [24] und Huntington-Krankheit [25] aufgezeigt; bei beiden handelt es sich um fortschreitende degenerative Erkrankungen, die in erster Linie das Gehirn betreffen (wenn auch nicht ausschließlich – bei beiden Erkrankungen ist eine muskuläre Komponente vorhanden). Zukünftige Forschungen könnten noch Zusammenhänge zwischen abnormalen EMG-Aufzeichnungen und der Erkrankung aufzeigen und damit einen weiteren Weg zur Diagnose eröffnen.
EMG-Geräte sind zwar nicht-invasiv und oft tragbar, erfordern jedoch einen gewissen Aufwand bei der Vorbereitung (sowohl hinsichtlich der Hautvorbereitung als auch der Erfassung einer Basislinie der Muskelaktivität); dennoch werden diese Geräte, ähnlich wie EEG-Geräte, bereits routinemäßig im klinischen Umfeld eingesetzt.
Analyse des Gesichtsausdrucks
Die Erzeugung von Gesichtsausdrücken ist oft ein automatischer, unbewusster Vorgang, kann aber auch bewusst gesteuert werden. Bei Menschen mit Autismus wurden Unterschiede in der Fähigkeit zur Erzeugung von Gesichtsausdrücken festgestellt [31].
Die Analyse von Gesichtsausdrücken wird auch im Zusammenhang mit Trainingsprogrammen für Menschen mit Autismus zur Verbesserung ihrer sozialen Fähigkeiten häufig diskutiert [32]. Auch wenn dies nicht direkt mit der Diagnose von Autismus zusammenhängt, könnten die aus einem solchen System gewonnenen Erkenntnisse dazu beitragen, das Verständnis dafür zu vertiefen, wie Autismus entsteht.
Forscher haben eine Methode vorgeschlagen, bei der automatisierte Gesichtsausdrucksanalysen zur Erkennung von Merkmalen der Schizophrenie eingesetzt werden [33]. Schizophrenie geht häufig mit einer gestörten Emotionsäußerung oder einem flachen Affekt einher, was letztlich bedeutet, dass sich die gezeigten Gesichtsausdrücke im Vergleich zu nicht-schizophrenen Kontrollpersonen unterscheiden können. Die Forscher stellen fest, dass das System signifikante Unterschiede zwischen diesen Personengruppen erkennen kann und als unterstützendes Instrument für die Diagnostik weiterentwickelt werden könnte.

Da die automatisierte Analyse von Gesichtsausdrücken völlig unauffällig ist, kann sie ohne jegliche Beeinträchtigung für die Patienten eingesetzt werden. Zwar sind weitere Untersuchungen erforderlich, um mögliche Zusammenhänge mit Autismus oder psychiatrischen Störungen eindeutig zu klären, doch dank ihrer einfachen Handhabung könnte diese Methode problemlos im klinischen Umfeld angewendet werden.
Ebenso bietet die menschliche Stimme eine weitere unaufdringliche und wertvolle Datenquelle für das Verständnis neurologischer und psychiatrischer Erkrankungen. Erfahren Sie mehr über das Potenzial der **Stimmenanalyse** als neue Dimension in der medizinischen Diagnostik.
Galvanische Hautreaktion
Die GSR (galvanische Hautreaktion), auch bekannt als EDA (elektrodermale Aktivität), ist ein Maß für die Aktivität der Schweißdrüsen, die häufig (aber nicht ausschließlich) an den Fingern gemessen wird. Diese Methode ist einfach anzuwenden, und die Geräte können tragbar sein, was eine naturgetreue Datenerfassung ermöglicht.
Es wurden (ähnlich wie bei der Analyse von Gesichtsausdrücken) auch Zusammenhänge mit Schizophrenie festgestellt, wenn auch mit Unstimmigkeiten, die möglicherweise auf diagnostische Klassifikationen zurückzuführen sind [27, 28]. Weitere Forschungen könnten Aufschluss darüber geben, ob und wie GSR/EDA nützliche Informationen für die Diagnose von Schizophrenie liefern können.
Es wurden signifikante Zusammenhänge mit dem Stresslevel einer Person festgestellt (neben der mittels EKG erfassten Herzfrequenz [26]). Auch wenn es sich hierbei nicht um eine psychiatrische Störung handelt, kann dies im klinischen Kontext eine relevante Information sein, die erfasst werden sollte.

Ähnlich uneinheitliche Ergebnisse wurden auch bei der Verwendung von GSR/EDA als Indikator für Autismus festgestellt [29]; dennoch wird im Rahmen groß angelegter Forschungsprojekte weiter daran gearbeitet, zuverlässige und praxistaugliche Biomarker zu identifizieren [30]. Das Forschungsprojekt JAKE (das wir bereits zuvor erörtert haben) könnte dazu beitragen, weitere Einblicke in die Ergebnisse von EEG-, Gesichtsausdrucksanalyse-, GSR- und Eye-Tracking-Daten zu gewinnen und zu verstehen, inwiefern diese jeweils mit Autismus zusammenhängen.
GSR-/EDA-Geräte lassen sich leicht anwenden, sind relativ kostengünstig und können als tragbare Geräte getragen werden, ohne die normalen Bewegungsabläufe nennenswert zu beeinträchtigen. Dies könnte eine ambulante und naturgetreue Datenerhebung ermöglichen, um mögliche Zusammenhänge mit psychiatrischen Störungen weiter zu untersuchen.
Fazit
Ein wesentlicher Vorteil dieser Geräte besteht darin, dass die Daten von jedem einzelnen Gerät gleichzeitig erfasst werden können. Angesichts der zunehmenden Anwendung von Methoden des maschinellen Lernens auf komplexe Datensätze ist es gut vorstellbar, dass solche Analysen den Weg für eine stärker automatisierte Erkennung einer Reihe potenzieller Krankheiten oder Störungen ebnen könnten.
Eine Kombination dieser Methoden könnte die Zuverlässigkeit der einzelnen Ergebnisse weiter erhöhen (z. B. durch die Analyse von EEG- und Eye-Tracking-Daten zur Früherkennung von Autismus bei Kindern, was sich nach vorläufigen Ergebnissen als lohnenswert erweisen könnte [34]).
Die oben genannten Studien stellen nur einige der Fälle dar, in denen mögliche Zusammenhänge zwischen den von diesen Geräten erfassten Daten und neurologischen Erkrankungen oder Störungen festgestellt wurden. Auch wenn in vielen Fällen weitere Studien erforderlich sind, um eindeutige Biomarker zu ermitteln, zeigt der Verlauf der aktuellen Forschung deutlich, dass dies die Richtung ist, in die wir uns bewegen.
Ich hoffe, es hat Ihnen gefallen, zu lesen, wie verschiedene Sensoren Einblicke in neurologische Erkrankungen und psychiatrische Störungen liefern können. Klicken Sie hier, um mehr darüber zu erfahren, wie iMotions dazu beitragen kann, ein besseres Verständnis für Fragestellungen in der medizinischen Forschung und im Gesundheitswesen zu entwickeln.
Literaturverzeichnis
[1] Harezlak, K., Kasprowski, P. (2018). Einsatz von Eye-Tracking in der Medizin: eine Übersicht, Forschungsfragen und Herausforderungen. Computerized Medical Imaging and Graphics. Apr.; 65:176–190.
[2] Diefendorf, A. R., Dodge, R. (1908). Eine experimentelle Untersuchung der Augenreaktionen von Geisteskranken anhand fotografischer Aufzeichnungen. Brain, Band 31, Ausgabe 3, 1, 451–489, https://doi.org/10.1093/Brain/31.3.451
[3] Arolt, V., Lencer, R., Nolte, A., Müller-Myhsok, B., Purmann, S., Schürmann, M. et al. (1996). Eine Störung der Blickverfolgung ist ein mutmaßlicher phänotypischer Anfälligkeitsmarker für Schizophrenie und lässt sich in Familien mit multiplem Auftreten der Erkrankung auf einen Locus auf Chromosom 6p zurückführen. Am. J. Med. Genet. 67, 564–579.
[4] García-Blanco, A., Salmerón, L., Perea, M., Livianos, L. (2014). Aufmerksamkeitsverzerrungen gegenüber emotionalen Bildern in den verschiedenen Phasen der bipolaren Störung: eine Eye-Tracking-Studie. Psychiatry Res. 215 (3), 628–633.
[5] Yang, Q., Wang, T., Su, N., Xiao, S., Kapoula, Z. (2013). Spezifische Defizite bei Sakkaden bei Patienten mit Alzheimer-Krankheit im leichten bis mittelschweren Stadium und bei Patienten mit amnestischer leichter kognitiver Beeinträchtigung. Age. 35 (4), 1287–1298.
[6] Crutcher, M. D., Calhoun-Haney, R., Manzanares, C. M., Lah, J. J., Levey, A. I., Zola, S. M. (2009). Blickverfolgung während einer visuellen Paarvergleichsaufgabe als Prädiktor für eine frühzeitige Demenz. Am. J. Alzheimer’s Dis. Other Dementias.
[7] Derwenskus, J., Rucker, J.C., Serra, A., Stahl, J. S., Downey, D. L., Adams, N. L., Leigh, R. (2005). Abnormale Augenbewegungen sagen Behinderungen bei MS voraus: Zweijährige Nachbeobachtung. Ann. N. Y. Acad. Sci. 1039 (1), 521–523.
[8] Wang, S., Jiang, M., Duchesne, X.M., Laugeson, E.A., Kennedy, D.P., Adolphs, R., Zhao, Q. (2015). Atypische visuelle Auffälligkeit bei Autismus-Spektrum-Störungen, quantifiziert mittels modellbasierter Eye-Tracking-Untersuchung. Neuron. 88 (3), 604–616.
[9] Jones, W., Carr, K., Klin, A. (2008). Das Fehlen eines bevorzugten Blickkontakts zu den Augen sich nähernder Erwachsener sagt den Grad der sozialen Beeinträchtigung bei 2-jährigen Kleinkindern mit Autismus-Spektrum-Störung voraus. Arch. Gen. Psychiatry. 65, 946–954. 10.1001/archpsyc.65.8.946
[10] Tseng, P.-H., Cameron, I. G., Pari, G., Reynolds, J. N., Munoz, D. P., Itti, L. (2013). Hochdurchsatz-Klassifizierung klinischer Populationen anhand natürlicher Blickbewegungen. J. Neurol. 260 (1), 275–284.
[11] Dankner, Y., Shalev, L., Carrasco, M., Yuval-Greenberg, S. (2017). Prestimulus-Hemmung von Sakkaden bei Erwachsenen mit und ohne Aufmerksamkeitsdefizit-/Hyperaktivitätsstörung als Indikator für zeitliche Erwartungen. Psychological Science. 28(7), 835–850.
[12] Petersen, R. (2009). Früherkennung der Alzheimer-Krankheit: Ist MCI zu spät? Current Alzheimer Research. 6(4):324–330. doi: 10.2174/156720509788929237.
[13] Pereira, M. L., Camargo, M., Aprahamian, I., Forlenza, O. V. (2014). Augenbewegungsanalyse und kognitive Verarbeitung: Erkennung von Indikatoren für die Entwicklung einer Alzheimer-Erkrankung. Neuropsychiatr Dis Treat. 10:1273–1285. doi: 10.2147/NDT.S55371.
[14] Mormann, F., Kreuz, T. H., Rieke, C. H., Andrzejak, R. G., Kraskov, A., David, P., Elger, C. E., Lehnertz, K. (2005). Zur Vorhersagbarkeit epileptischer Anfälle. Clin Neurophysiol. 116:569–97.
[15] Kowalski, J. W., Gawel, M., Pfeffer, A., Barcikowska, M. (2001). Der diagnostische Wert des EEG bei der Alzheimer-Krankheit: Korrelation mit dem Schweregrad der geistigen Beeinträchtigung. Journal of Clinical Neurophysiology. 18(6): 570–575.
[16] Cociu, B. A., Das, S., Billeci, L., Jamal, W., Maharatna, K., Calderoni, S., Narzisi, A., Muratori, F. (2017). Multimodale Analyse der funktionellen und strukturellen Konnektivität des Gehirns bei Autismus: Ein vorläufiger integrierter Ansatz mit EEG, fMRT und DTI. IEEE Trans. Cogn. Develop. Syst. 10, 2, 213–226. DOI: 10.1109/TCDS.2017.2680408.
[17] Arns, M., Conners, C. K., Kraemer, H. C. (2013). Ein Jahrzehnt der Forschung zum EEG-Theta-Beta-Verhältnis bei ADHS: eine Metaanalyse. J. Atten. Disord. 17, 374–383. 10.1177/1087054712460087.
[18] Boutros, N. N., Arfken, C., Galderisi, S., Warrick, J., Pratt, G., Iacono, W. (2008). Der Stellenwert spektraler EEG-Anomalien als diagnostisches Kriterium für Schizophrenie. Schizophr. Res. 99, 225–237.
[19] Kam, J. W., Bolbecker, A. R., O’Donnell, B. F., Hetrick, W. P., Brenner, C. A. (2013). Anomalien der EEG-Leistung und Kohärenz im Ruhezustand bei bipolarer Störung und Schizophrenie. J Psychiatr Res. 47:1893–901. doi: 10.1016/j.jpsychires.2013.09.009.
[20] Velikova, S., Locatelli, M., Insacco, C., Smeraldi, E., Comi, G., Leocani, L. (2010). Dysfunktionale Hirnschaltkreise bei Zwangsstörungen: Quellen- und Kohärenzanalyse von EEG-Rhythmen. Neuroimage. 49(1):977–983.
[21] Zerr, I., Pocchiari, M., Collins, S., Brandel, J. P., de Pedro, C. J., Knight, R. S. et al. (2000). Analyse von 14-3-3-Proteinen im EEG und Liquor als Hilfsmittel zur Diagnose der Creutzfeldt-Jakob-Krankheit. Neurology. 55:811–815. doi: 10.1212/WNL.55.6.811.
[22] Herrmann, C., Demiralp, T. (2005). Gamma-Oszillationen im menschlichen EEG bei neuropsychiatrischen Störungen. Clin. Neurophysiol. 116, 2719–2733. doi: 10.1016/j.clinph.2005.07.007
[23] Kishnani, P. S., Steiner, R. D., Bali, D., Berger, K., Byrne, B. J., Case, L., Crowley, J. F., Downs, S., Howell, R. R., Kravitz, R. M., Mackey, J., Marsden, D., Martins, A. M., Millington, D. S., Nicolino, M., O’Grady, G., Patterson, M. C., Rapoport, D. M., Slonim, A., Spencer, C. T., Tifft, C. J., Watson, M. S. (2006). Leitlinie zur Diagnose und Behandlung der Pompe-Krankheit. Genet Med. 8:267–288. doi: 10.1097/01.gim.0000218152.87434.f3.
[24] Vitale, C., Marcelli, V., Furia, T. et al. (2011). Vestibuläre Beeinträchtigung und adaptives Haltungsungleichgewicht bei Parkinson-Patienten mit lateraler Rumpfbeugung. Mov Disord. 26:1458–1463.
[25] Swerdlow, N. R., Paulsen, J., Braff, D. L. et al. (1995). Beeinträchtigte Präpuls-Inhibition der akustischen und taktilen Schreckreaktion bei Patienten mit Huntington-Krankheit. J. Neurol. Neurosurg. Psychiatry. 58, 192–200.
[26] Tulen, J. H. M., Moleman, P., Van Steenis, H. G., Boomsma F. (1989). Charakterisierung von Stressreaktionen auf den Stroop-Farbwort-Test. Pharmacol. Biochem. Behav. 32, 9–15. 10.1016/0091-3057(89)90204-9.
[27] Öhman, A. (1981). Elektrodermale Aktivität und Anfälligkeit für Schizophrenie: eine Übersicht. Biol. Psychol. 12, 87–145. 10.1016/0301-0511(81)90008-9.
[28] Zahn, T. P., Frith, C. D., Steinhauer, S. R. (1991). Autonome Funktionen bei Schizophrenie: Hautleitfähigkeit, Herzfrequenz, Pupillographie. In S. R. Steinhauer, J. H. Gruzelier & J. Zubin (Hrsg.), Handbuch der Schizophrenie: Band 5. Neuropsychologie, Psychophysiologie und Informationsverarbeitung (S. 185–224). Amsterdam: Elsevier.
[29] Hirstein, W., Iversen, P., Ramachandran, V. S. (2001). Autonome Reaktionen autistischer Kinder auf Menschen und Gegenstände. Proc Biol Sci. 268(1479):1883–8.
[30] Ness, S. L., Manyakov, N. V., Bangerter, A. et al. (2017). JAKE(R) Multimodal Data Capture System: Erkenntnisse aus einer Beobachtungsstudie zu Autismus-Spektrum-Störungen. Front Neurosci. 11:517.
[31] Manfredonia, J., Bangerter, A., Manyakov, N. V., Ness, S., Lewin, D., Skalkin, A., Boice, M., Goodwin, M. S., Dawson, G., Hendren, R., Leventhal, B., Shic, F., Pandina, G. (2018). Automatische Erkennung von gestellten Gesichtsausdrücken bei Personen mit Autismus-Spektrum-Störung. J Autism Dev Disord. 8. Okt. doi: 10.1007/s10803-018-3757-9.
[32] Liu, R., Salisbury, J. P., Vahabzadeh, A., Sahin, N. T. (2017). Machbarkeit eines auf Autismus ausgerichteten Augmented-Reality-Smart-Glasses-Systems für soziale Kommunikation und Verhaltenscoaching. Front. Pediatr. 5:145. doi: 10.3389/fped.2017.00145.
[33] Wang, P., Barrett, F., Martin, E., Miloncva, M., Gur, R. E., Gur, R. C. et al. (2008). Automatisierte videobasierte Analyse von Gesichtsausdrücken bei neuropsychiatrischen Störungen. Journal of Neuroscience Methods. 168: 224–238.
[34] Billeci, L., Narzisi, A., Tonacci, A., Sbriscia-Fioretti, B., Serasini, L., Fulceri, F., Apicella, F., Sicca, F., Calderoni, S., Muratori, F. (2017). Ein integrierter EEG- und Eye-Tracking-Ansatz zur Untersuchung der Reaktion auf und der Initiierung von gemeinsamer Aufmerksamkeit bei Autismus-Spektrum-Störungen. Scientific Reports, 7(1):13560.